Konzentration
 PharmaWikiDie Konzentration (C) ist eine Gehaltsangabe. Sie gibt zum Beispiel an, welche Masse einer Substanz in einem bestimmten Volumen gelöst vorliegt. In der Pharmazie werden Konzentrationen vor allem für flüssige und halbfeste Arzneiformen verwendet.
PharmaWikiDie Konzentration (C) ist eine Gehaltsangabe. Sie gibt zum Beispiel an, welche Masse einer Substanz in einem bestimmten Volumen gelöst vorliegt. In der Pharmazie werden Konzentrationen vor allem für flüssige und halbfeste Arzneiformen verwendet.synonym: C
DefinitionEine Konzentration (C) gibt den Gehalt eines Stoffes in einem anderen als Quotient an. Per Definition ist damit die Menge eines Stoffes gemeint, die in einem bestimmten Volumen vorliegt. Konzentrationen können sich aber auch auf Massen beziehen.
In der Pharmazie wird die Konzentration häufig im Zusammenhang mit flüssigen und halbfesten Darreichungsformen verwendet. Bei festen Arzneiformen wie Tabletten oder Kapseln ist die Angabe der Masse der Wirkstoffe gebräuchlicher.
MassenkonzentrationEine Oxycodon-Lösung zum Einnehmen enthält zum Beispiel 10 Milligramm (mg) wasserfreies Oxycodonhydrochlorid pro Milliliter (ml): 10 mg/ml.
Bei diesem Beispiel handelt es sich um die sogenannten Massenkonzentration mit der Einheit Gramm pro Liter (g/L, also m/V).
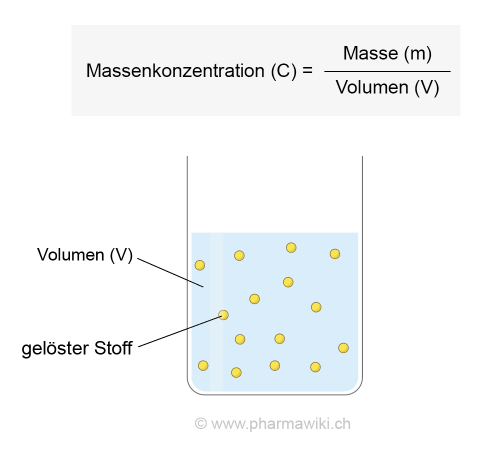
Massenkonzentration (C) = Masse (m) / Volumen (V)
Massenkonzentration, zum Vergrössern anklicken. Illustration © PharmaWiki
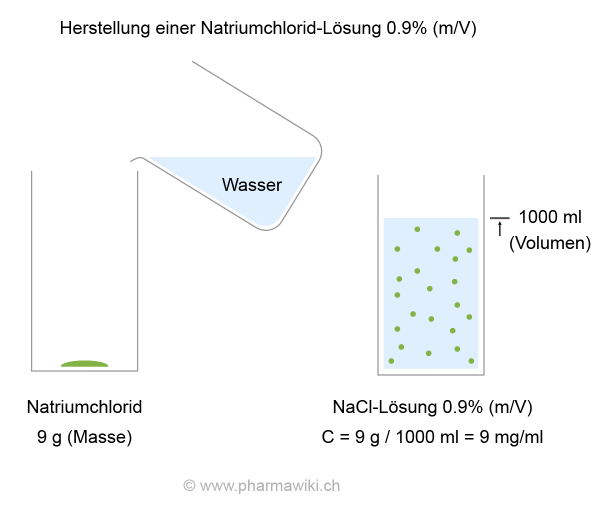
Eine physiologische Kochsalzlösung enthält 9 g Natriumchlorid (Masse) auf 1 Liter Wasser (Volumen). Ihre Konzentration wird meistens prozentual angegeben: 0.9%. Sie beträgt 9 g/L oder 9 mg/ml. Für die Herstellung werden 9 g Natriumchlorid abgewogen und auf 1000 ml (nicht Gramm!) ergänzt. Zur Bestimmung des Volumens kann zum Beispiel ein Messzylinder verwendet werden (siehe unter Glaswaren in der Chemie).
Herstellung einer Natriumchlorid-Lösung 0.9%, zum Vergrössern anklicken. Illustration © PharmaWiki
MassenprozentEs können auch zwei Massen aufeinander bezogen werden. So enthalten beispielsweise 100 g eines Diclofenac-Gels 1 g Diclofenac-Natrium. Die Konzentration beträgt 1% oder 10 mg/g (m/m).
Wird ein solches Gel zubereitet, muss nicht mit Volumen gearbeitet werden. Das Gel besteht aus 1 g Wirkstoff und 99 g Grundlage. Die Komponenten können mit einer Waage gewogen werden. Beachten Sie den Unterschied zum obigen Beispiel.
VolumenkonzentrationBei der Volumenkonzentration werden zwei Volumen aufeinander bezogen. Die Einheit ist L/L. Die Prozentangaben von Ethanol beziehen sich häufig auf das Volumen.
100 ml Ethanol 20% (V/V) bedeutet, dass in dieser Zubereitung 20 ml reiner (wasserfreier) Alkohol enthalten sind.
Vorsicht: Volumen mit unterschiedlicher Dichte können nicht addiert werden! Siehe unter → Verdünnungen.
StoffmengenkonzentrationBei der Stoffmengenkonzentration (Molarität) wird die Menge der Substanz in der Stoffmenge (mol) angegeben, also der Anzahl der enthaltenen Teilchen. Die Einheit ist mol pro Liter (mol/L), offiziell gemäss SI: mol/m3.
Eine 1-molare Lösung enthält 1 Mol der Substanz in 1 Liter Wasser. Dies wird auch als 1 M bezeichnet.
Ein → Mol einer Substanz entspricht 6.022 140 76 × 1023 Teilchen (= Avogadro-Zahl).
- C (Stoffmengenkonzentration) = n (Stoffmenge) / V (Volumen)
Wirkstoffe sind in vielen Arzneimitteln in Form von → Salzen (→ Wirkstoffsalzen) enthalten. Da diese eine andere (höhere) Molekülmasse als der Wirkstoff haben, unterscheiden sich die Konzentrationen in Bezug auf den Wirkstoff und sein Salz. Im obigen Beispiel mit Oxycodon beträgt die Konzentration der reinen Oxycodonbase nur 9 mg/ml statt 10 mg/ml (Salz). Dies kann bei der Dosierung eine Rolle spielen. Siehe auch unter → Wirkstoffsalze.
KonzentrationsveränderungenWird der enthaltene Stoff oder das Volumen verändert, also beispielsweise erhöht oder reduziert, verändert sich die Konzentration. Ist also beispielsweise 1 g Natriumchlorid in 1000 ml Wasser enthalten, beträgt die Konzentration 1 g/L. Wird mit Wasser auf 2 Liter ergänzt, beträgt die Konzentration nur noch 0.5 g/L.
Für Berechnungen im Zusammenhang mit Verdünnungen gibt es die folgende Formel, das sogenannte Mischungskreuz:
- C1 (Konzentration 1) x V1 (Volumen 1) = C2 (Konzentration 2) x V2 (Volumen 2)
C: Prozent oder Stoffmengenkonzentration
Ausführliche Informationen finden Sie im Artikel → Verdünnungen
Rechnen mit KonzentrationenBeispiel:
Eine Ibuprofen-Suspension enthält 20 mg/ml Ibuprofen. Sie möchten einem fünfjährigen Kind eine Einzeldosis von 100 mg Ibuprofen gegen Fieber verabreichen. Wie viel Suspension benötigen Sie?
Lösung: 5 ml
siehe auchPlasmakonzentration, Masse, Volumen, Stoffmenge, Dichte, Verdünnungen
Literatur- Europäisches Arzneibuch PhEur
- Fachliteratur
- Lehrbücher der Chemie
- Lehrbücher der pharmazeutischen Technologie
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.