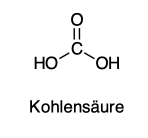
Kohlensäure
 Arzneimittelgruppen
Arzneimittelgruppen  Säuren
Säuren  CarbonsäurenDie Kohlensäure ist eine schwache und zweiprotonige Säure, die trotz des Kohlenstoffatoms zu den anorganischen Verbindungen gezählt wird. Sie wird im Wasser bei der Lösung von Kohlenstoffdioxid gebildet, zerfällt aber rasch wieder. In der Pharmazie spielen vor allem die Salze der Kohlensäure eine wichtige Rolle, d.h. die Hydrogencarbonate und die Carbonate.
CarbonsäurenDie Kohlensäure ist eine schwache und zweiprotonige Säure, die trotz des Kohlenstoffatoms zu den anorganischen Verbindungen gezählt wird. Sie wird im Wasser bei der Lösung von Kohlenstoffdioxid gebildet, zerfällt aber rasch wieder. In der Pharmazie spielen vor allem die Salze der Kohlensäure eine wichtige Rolle, d.h. die Hydrogencarbonate und die Carbonate.synonym: Carbonic acid, Dihydrogencarbonat, H2CO3
ProdukteDie Kohlensäure ist in sehr geringen Mengen zum Beispiel im Mineralwasser (Sprudelwasser) und in Limonaden enthalten.
Struktur und EigenschaftenDie Kohlensäure (H2CO3, Mr = 62.0 g/mol) ist eine schwache, zweiprotonige Säure, die trotz des Kohlenstoffatoms zu den anorganischen Verbindungen gezählt wird. Sie ist in Gegenwart von Wasser sehr instabil und deshalb war früher nicht klar, ob sie überhaupt existiert. Sie ist unter speziellen Bedingungen jedoch als Reinsubstanz isolier- und kristallisierbar und in Abwesenheit von Wasser erstaunlich stabil.
Die Salze der Kohlensäure werden als Carbonate (CO32-, ohne Wasserstoffatome) und Hydrogencarbonate (HCO3-, Bicarbonate, mit 1 Wasserstoffatom) bezeichnet. Dazu gehören zum Beispiel Calciumcarbonat (Kalk), Natriumcarbonat (Soda), Kaliumcarbonat (Pottasche) und Natriumhydrogencarbonat (Natron).
Die Kohlensäure entsteht, wenn Kohlenstoffdioxid (CO2) in Wasser gelöst wird. Dabei bildet sich das folgende Gleichgewicht:
- CO2 (Kohlenstoffdioxid) + H2O (Wasser) ⇌ H2CO3 (Kohlensäure)
Die Lösung des Kohlenstoffdioxids wird von einem erhöhten Druck und einer tiefen Temperatur begünstigt. Die Reaktion führt aufgrund der Deprotonierung zu einer leichten Ansäuerung des Wassers:
- H2CO3 ⇌ HCO3- + H+ ⇌ CO32- + H+
Die Kohlensäure ist im Wasser sehr instabil und zerfällt rasch. Wasser „mit Kohlensäure“ (im Deutschen: „Sprudel“) wird durch Einleitung von Kohlenstoffdioxid hergestellt. Wird die Flasche geöffnet, sinkt der Druck und sie beginnt zu sprudeln, d.h. das Gas wird wieder freigesetzt. Der pH-Wert liegt bei gewöhnlichem Sprudel bei etwa 5.5, bei einem geringeren CO2-Gehalt steigt er auf Werte zwischen 6 bis 7 an. Neben der Drucksenkung führt auch eine Temperaturerhöhung oder das Schütteln der Flasche zur Freisetzung des Kohlendioxids. Durch die Zugabe von Säuren oder Basen kann das Gleichgewicht verschoben werden.
Der Kohlensäuregehalt ist im Sprudelwasser sehr gering. Im Restaurant sollte also eigentlich „Wasser mit Kohlenstoffdioxid“ bestellt werden. Denn weit über 99 % des Kohlenstoffdioxids sind im Wasser gelöst.
Die Kohlensäure ist wichtig für Puffersysteme im menschlichen Körper, für den Säure-Base-Haushalt und für die Einstellung des pH-Werts des Bluts. Sie spielt auch eine zentrale Rolle beim Transport von Kohlenstoffdioxid aus der Peripherie zur Lunge. CO2 entsteht bei der ATP-Produktion in den Mitochrondrien.
Zur Beschleunigung der Reaktion zwischen Kohlenstoffdioxid, Kohlensäure und Bicarbonat existieren im menschlichen Körper Enzyme, die Carboanhydrasen.
AnwendungsgebieteIn der Pharmazie spielen vor allem die Carbonate und Hydrogencarbonate eine wichtige Rolle, zum Beispiel als Hilfsstoffe, für die Behandlung von Magenbrennen und für die Herstellung von Wirkstoffsalzen.
siehe auchSäuren, Kohlenstoffdioxid, Getränke
Literatur- Lehrbücher der Chemie
- Loerting T. et al. On the Surprising Kinetic Stability of Carbonic Acid. Angew Chem Int Ed Engl, 2000, 39(5), 891-894 Pubmed

- Wissenschaftliche Fachliteratur
- Quellen
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
