Zulassung von Arzneimitteln
 PharmaWiki
PharmaWikisynonym: Registrierung, Marktzulassung
Zulassung von ArzneimittelnDamit ein Arzneimittel in einem Land in den Verkehr gebracht werden darf, ist ein Verfahren bei der zuständigen Arzneimittelbehörde erforderlich. In der Schweiz ist das beispielsweise die Swissmedic, in Deutschland das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), in Österreich das Bundesamt für Sicherheit im Gesundheitswesen (BASG) und in den USA die Food and Drug Administration (FDA). Die Zulassung muss für jedes Land einzeln beantragt werden. In der EU ist auch eine zentrale Zulassung bei der European Medicines Agency (EMA) möglich. Ist das Arzneimittel bereits in einem anderen Land registriert, können die Ergebnisse berücksichtigt werden.
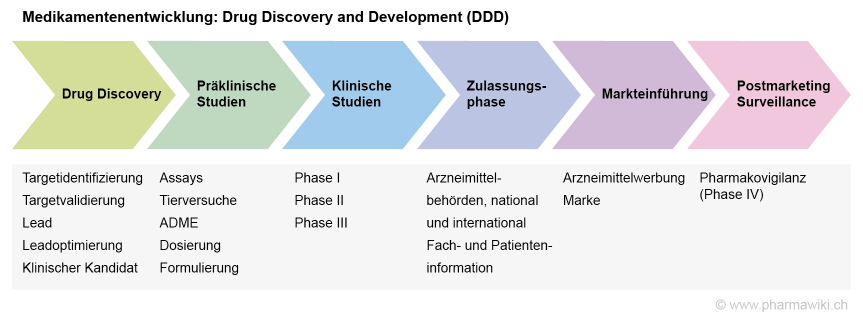
Medikamentenentwicklung, zum Vergrössern anklicken. Illustration © PharmaWiki
Die Grundlage für die Zulassung sind die wissenschaftlichen Untersuchungen, die präklinischen Studien und die klinischen Phase-I- bis Phase-III-Studien, welche vorgängig durchgeführt wurden. Falls die klinischen Studien ihre Endpunkte nicht erreicht haben, ist eine Zulassung unwahrscheinlich.
Die Zulassung beinhaltet auch die Patienteninformation und die Fachinformation, welche das Arzneimittel begleiten. Die darin enthaltenen Angaben wie die Dosierung, die Anwendungsgebiete und die Vorsichtsmassnahmen können deshalb nur in Absprache mit der Behörde geändert oder erweitert werden. Aufgrund der nationalen Registrierung können sich diese Informationen international unterscheiden.
Die Zulassung kann aufgehoben oder eingeschränkt werden, wenn neue Erkenntnisse bezüglich der Arzneimittelqualität, der Wirkungen, Risiken und unerwünschten Wirkungen bekannt werden. Falls also beispielsweise eine neue klinische Studie eine unzureichende Wirksamkeit zeigt oder den Arzneimittelbehörden wiederholt schwere unerwünschte Wirkungen gemeldet werden. Die Zulassungsinhaberin kann auch freiwillig auf eine Zulassung verzichten, falls der kommerzielle Erfolg ausbleibt oder die Produktion nicht mehr möglich ist.
Weshalb ist eine Zulassung erforderlich? Medikamente sind keine normalen Konsumgüter. Sie sind hoch wirksam, können unerwünschte Wirkungen und bei einer falschen Dosierung Vergiftungen auslösen. Ihre Wirksamkeit, die Qualität, die Unbedenklichkeit und die Sicherheit müssen zuverlässig nachgewiesen sein. Die Zulassung ist auch eine wichtige Voraussetzung dafür, dass ein Medikament von den Krankenversicherungen vergütet wird. Sie ist aber keine Garantie, weil dafür eine andere Behörde zuständig ist. In der Schweiz ist es das Bundesamt für Gesundheit.
Für einige Arzneimittel ist eine vereinfachte Zulassung möglich. Zum Beispiel für Generika (Nachahmerpräparate), Biosimilars und Medikamente der Alternativmedizin.
Lebensmittel, Nahrungsergänzungsmittel und Medizinprodukte können einfacher und kostengünstiger in den Handel gebracht werden und es keine Arzneimittelzulassung erforderlich.
Auch nach der Markteinführung werden Medikamente weiterhin überwacht. Dies wird als Pharmakovigilanz oder als Post-Marketing Surveillance bezeichnet. So werden medizinische Fachpersonen angehalten, Nebenwirkungen der Behörde zu melden.
siehe auchArzneimittel, Medikamentenentwicklung, Drug Discovery, Klinische Studien, Markteinführung
Literatur- Arzneimittelbehörden
- Fachliteratur
- Heilmittelgesetzgebung
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.