Dissoziationskonstante
 PharmakodynamikDefinition und Eigenschaften
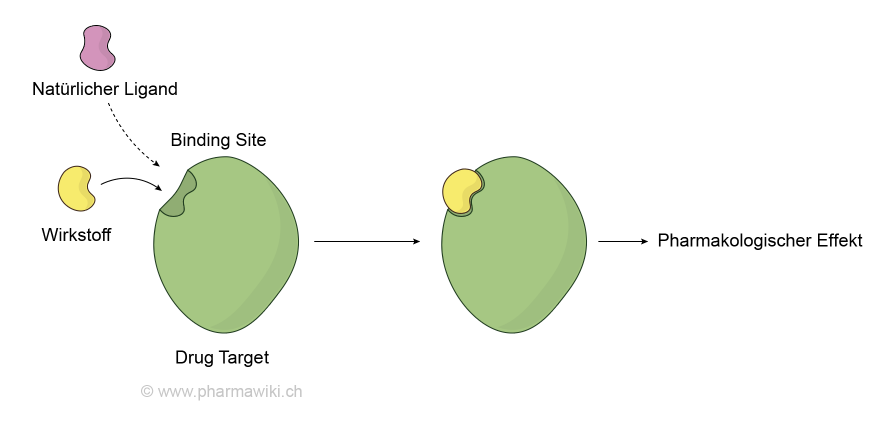
PharmakodynamikDefinition und EigenschaftenDamit ein Medikament seine pharmakologischen Effekte ausüben kann ist, müssen die darin enthaltenen Wirkstoffe in der Regel an molekulare Zielstrukturen im Organismus binden, die sogenannten Drug Targets. Das sind zum Beispiel Rezeptoren, Enzyme, Transporter, Ionenkanäle und Nukleinsäuren. Diese Bindung wird für Rezeptoren formal so dargestellt:
W(irkstoff) + R(ezeptor) ⇌ Wirkstoff-Rezeptor-Komplex (WR)
Die Dissoziationskonstante ist eine Gleichgewichtskonstante, die angibt, wo das Gleichgewicht dieses Prozesses liegt und das Verhältnis von gebundenem und ungebundenem Wirkstoff angibt. Sie ist wie folgt definiert (C = Konzentration, in mol/L):
KD = C(W) · C(R) / C(WR)
Die Einheit von KD ist mol/L und kann auch mit M angegeben werden. Je kleiner der Wert ist, desto mehr Wirkstoff liegt an den Rezeptor gebunden vor und desto höher ist die Bindungsaffinität des Wirkstoffs. Eine möglichst starke Bindung ist in der Regel auch eine Voraussetzung für die Wirksamkeit. Eine gute Bindungsstärke liegt im nanomolaren Bereich (z.B. 1 nM = 1 nmol/L).
Bindung eines Wirkstoffs an sein Drug Target, zum Vergrössern anklicken. Illustration © PharmaWiki
siehe auchAgonisten, Antagonisten, Bindungsaffinität, Rezeptoren, Intermolekulare Wechselwirkungen
AutorInteressenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
PharmaWiki mit Google durchsuchen.